Efectos del pretratamiento con Trichoderma y Bacillus en la germinación de semillas de Agave victoriae-reginae T. Moore
DOI:
https://doi.org/10.29298/rmcf.v13i69.844Palabras clave:
Agave, especie en riesgo, latencia, noha, tratamiento pregerminativo, viabilidad de semillaResumen
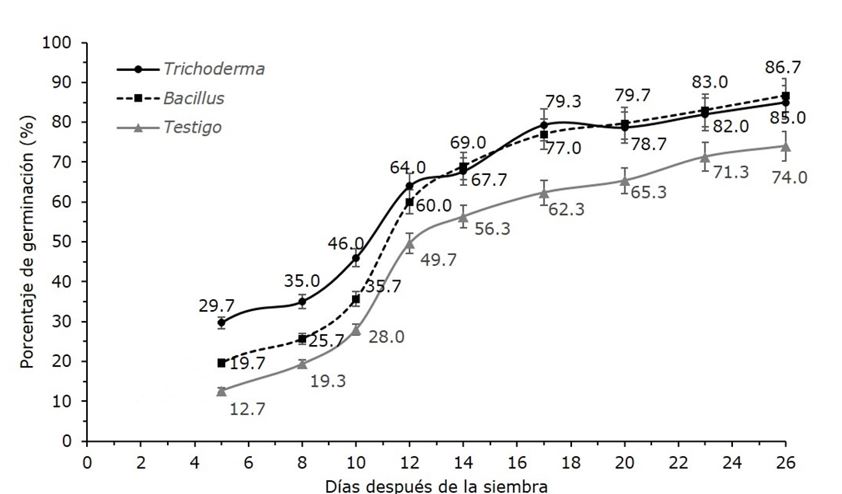
La aplicación de tratamientos pregerminativos es fundamental para mejorar las tasas de germinación de las semillas de especies forestales, entre los cuales el uso de microorganismos es uno de ellos. En este estudio se evaluó el porcentaje de germinación de semillas de Agave victoriae-reginae tratadas con Trichoderma spp. y Bacillus spp. Se probaron tres tratamientos: T1 (Trichoderma), T2 (Bacillus) y T3 (Testigo), con tres repeticiones de 100 semillas cada una. Las semillas se sumergieron en una solución de 1 × 106 UFC (tratamientos T1 y T2), y en agua corriente (T3), luego se sembraron sobre Sphagnum peat moss y se registró el porcentaje de germinación diariamente. La germinación comenzó a los 5 días después de la siembra, lo que significa que las semillas no presentaron latencia. Entre el 8° y 12° día se registró un aumento acelerado de la germinación en los tres casos, hasta que la el proceso finalizó a los 26 días, con 85 % de germinación total para semillas tratadas con Trichoderma, 86.7 % con Bacillus y 74 % con el testigo. Se observó un efecto significativo del tratamiento sobre el porcentaje de germinación; incluso el uso de ambos microorganismos aceleró el proceso de germinación con respecto al testigo. Estos resultados sugieren que el uso de Trichoderma spp y Bacillus spp. como tratamientos pregerminativos puede mejorar la germinación de A. victoriae-reginae y su conservación a largo plazo, lo que contribuye a la permanencia de esta especie en peligro de extinción.
Descargas
Citas
Ahmad, F., I. Ahmad and M. S. Khan. 2008. Screening of free-living rhizospheric bacteria for their multiple plant growth promoting activities. Microbiological Research 163(2):173-181. Doi:10.1016/j.micres.2006.04.001.
Barnett, J. P. and S. Varela. 2004. A review of chemical treatments to improve germination of longleaf pine seeds. Native Plants Journal 5(1):18-24. Doi:10.2979/NPJ.2004.5.1.18.
Cabra C., T., C. A. Rodríguez G., C. P. Villota C., O. A. Tapasco A. y A. Hernández R. 2017. Efecto de Bacillus sobre la germinación y crecimiento de plántulas de tomate (Solanum lycopersicum L). Acta Biológica Colombiana 22(1):37-44. Doi:10.15446/abc.v22n1.57375.
Castillo R., F., J. D. Sánchez C., S. E. Rangel E. y J. Canul K. 2014. Efecto de microorganismos en la promoción de la germinación de semillas de la cactácea Echinocactus platyacanthus Link & Otto. Interciencia 39(12):863-867. www.redalyc.org/articulo.oa?id=33932786006 (10 de abril de 2020).
Castillo Q., D., D. Y. Avila F., F. Castillo R., A. Antonio B. y O. U. Martínez B. 2015. Nolina cespitifera Trel. recurso forestal no maderable de importancia económica y social del noreste de México. Interciencia 40(9):611-617. https://www.redalyc.org/articulo.oa?id=33940998005 (3 de mayo de 2020).
Convention on International Trade in Endangered Species of Wild Fauna and Flora (CITES). 2017. Lista de especies CITES. https://bit.ly/3Fm2Esz (10 de agosto de 2020).
Cubillos H., J. G., A. Páez R. y L. Mejía D. 2011. Evaluación de la capacidad biocontroladora de Trichoderma harzianum Rifai contra Fusarium solani (Mart.) Sacc. asociado al complejo “Secadera” en Maracuyá, bajo condiciones de invernadero. Revista Facultad Nacional Agronomía Medellín 64(1): 5821-5830. http://www.scielo.org.co/pdf/rfnam/v64n1/a08v64n01.pdf (6 de mayo de 2020).
Delgado-Sánchez, P., M. A. Ortega-Amaro, J. F. Jiménez-Bremont and J. Flores. 2010. Are fungi important for breaking seed dormancy in desert species? Experimental evidence in Opuntia streptacantha (Cactaceae). Plant Biology 13(1):154-159. Doi:10.1111/j.1438-8677.2010.00333.x.
Delgado-Sánchez, P., J. F. Jiménez-Bremont, M. L. Guerrero-González and J. Flores. 2013. Effect of fungi and light on seed germination of three Opuntia species from semiarid lands of central Mexico. Journal of Plant Research 126: 643–649. Doi:10.1007/s10265-013-0558-2.
Díaz P., G., J. A. Ruíz C., G. Medina G., M. A. Cano G., V. Serrano A. e I. Sánchez C. 2007. Estadísticas climatológicas básicas del estado de Coahuila. (Periodo 1961 – 2003). Libro Técnico N° 16. Campo Experimental Cotaxtla. CIRGOC-INIFAP Medellín de Bravo, Ver., México. 159 p.
Donohue, K., L. Dorn, C. Griffith, E. Kim, A. Aguilera, C. R. Polisetty and J. Schmitt. 2005. The evolutionary ecology of seed germination of Arabidopsis thaliana: Variable natural selection on germination timing. Evolution 59(4): 758-770. Doi: 10.1111/j.0014-3820.2005.tb01751.x.
Doria, J. 2010. Generalidades sobre las semillas: Su producción, conservación y almacenamiento. Cultivos Tropicales 31(1):74-85. http://scielo.sld.cu/pdf/ctr/v31n1/ctr11110.pdf (5 de junio de 2020).
Durán, M. C. y H. G. Núñez P. 2015. Utilización de un sistema de inmersión temporal (SIT) para multiplicar plantas ornamentales de Agave victoriae-reginae. Jóvenes en la Ciencia 1(2): 66-71. http://www.jovenesenlaciencia.ugto.mx/index.php/jovenesenlaciencia/article/view/381 (13 de junio de 2020).
Freeman, C. E. 1975. Germination responses of a New Mexico population of Parry agave (Agave parryi Engelm. var. parryi) to constant temperature, water stress and pH. The Southwestem Naturalist 20(1):69-74. Doi: 10.2307/3670012.
Freeman, C. E., R. S. Tiffany and W. H. Reid. 1977. Germination responses of Agave lechuguilla, A. parryi, and Fouquieria splendens. The Southwestern Naturalist 22(2):195-204. Doi: 10.2307/3669810.
García, E. 1973. Modificaciones al sistema de clasificación climática de Köppen, Segunda Edición. Instituto de Geografía, UNAM. México, D.F., México. 146 p.
Gentry, H. S. 1982. Agaves of Continental Norht American. The University of Arizona Press. Tucson, AZ, USA. 670 p.
Gómez R., M., J. Villegas, J., C. Sáenz R, C. y R. Lindig C. 2013. Efecto de la micorrización en el establecimiento de Pinus pseudostrobus en cárcavas. Madera y Bosques 19(3):51-63. Doi: 10.21829/myb.2013.193327.
González E., M. S., M. González E., I. L. López E., L. Reséndiz R., J. A. Tena F. y F. I. Retana R. 2011. El complejo Agave victoriae-reginae (Agavaceae). Acta Botánica Mexicana 95:65-94. Doi: 10.21829/abm95.2011.268.
Guillen, C. R., F. D. Hernández C., G. Gallegos M., R: Rodríguez H., C. N. Aguilar G., E. Padrón C. y M. H. Reyes V. 2006. Bacillus spp. as biocontrol in infested soils with Fusarium spp., Rhizoctonia solani Kühn and Phytophthora capsici Leonina and its effect on development and yield of pepper (Capsicum annuum L.). Revista Mexicana de Fitopatología 23:105-113. https://www.redalyc.org/articulo.oa?id=61224204 (9 de mayo de 2020).
Hernández M., S., R. Novo S., M. A. Mesa P., A. Ibarra M. y D. Hernández R. 2017. Capacidad de Trichoderma spp. como estimulante de la germinación en maíz (Zea mays L.) y frijol (Phaseolus vulgaris L.). Revista de Gestión del Conocimiento y el Desarrollo Local 4(1):19-23. https://revistas.unah.edu.cu/index.php/RGCDL/article/view/898 (10 de agosto de 2020).
Khurana, E. and J. S. Singh. 2001. Ecology of seed and seedling growth for conservation and restoration of tropical dry forest: A review. Environmental Conservation 28(1):39-52. Doi:10.1017/S0376892901000042.
Moncaleano E., J., B. C. F. Silva, S. R. D. Silva, J. A. A. Granja, M. C. J. L. Alves and M. F. Pompelli. 2013. Germination responses of Jatropha curcas L. seeds to storage and aging. Industrial Crops and Products 44: 684-690. Doi:10.1016/j.indcrop.2012.08.035.
Moreno R., A., V. García M., J. L. Reyes C., J. Vásquez A. y P. Cano R. 2018. Rizobacterias promotoras del crecimiento vegetal: una alternativa de biofertilización para la agricultura sustentable. Revista Colombiana de Biotecnología 20(1):68-83. Doi: 10.15446/rev.colomb.biote.v20n1.73707.
Ortega, U., M. Duñabeitia, S. Menendez, C. González M. and J. Makada. 2004. Effectiveness of mycorrhizal inoculation in the nursery on growth and water relations of Pinus radiata in different water regimes. Tree Physiology 24: 65-73. Doi:10.1093/treephys/24.1.65.
Peña V., C. B., A. B. Sánchez U., J. R. Aguirre R., C. Trejo, E. Cárdenas and A. Villegas M. 2006. Temperature and mechanical scarification on seed germination of ´maguey´(Agave salmiana Otto ex Salm-Dyck). Seed Science and Technology 34: 47-56. Doi: 10.15258/sst.2006.34.1.06.
R Core Team. 2017. R project 4.3.4. https://www.r-project.org/ (16 de febrero de 2017).
Ramírez T., H. M., C. B. Peña V., J. R. Aguirre R., J. A. Reyes A., A. B. Sánchez U. and S. Valle G. 2012. Seed germination temperatures of eight Mexican Agave species with economic importance. Plant Species Biology 27:124-137. Doi: 10.1111/j.1442-1984.2011.00341.x.
Ramírez T., H. M., R. Niño V., J. R. Aguirre R., J. Flores, J. A. De-Nova V. and R. Jarquin G. 2016. Seed viability and effect of temperature on germination of Agave angustifolia subsp. tequilana and A. mapisaga; two useful Agave species. Genetic Resources and Crop Evolution 63: 881-888. Doi: 10.1007/s10722-015-0291-x.
Rangel L., S., A. Casas and P. Dávila. 2015. Facilitation of Agave potatorum: An ecological approach for assisted population recovery. Forest Ecology and Management 347:57-74. Doi: 10.1016/j.foreco.2015.03.003.
Sánchez U., A. B., I. Ortega, I. Cano, A. González, C. B. Peña V., G. Rivero, G. Sthormes y D. Pacheco. 2011. Efecto de la escarificación de la semilla y del sustrato sobre el crecimiento de plántulas de Agave salmiana. Revista de la Facultad de Agronomía 28: 40-50. https://produccioncientificaluz.org/index.php/agronomia/article/view/26979/27604 (20 de agosto de 2020).
Sánchez S., J., J. Flores, E. Jurado, J. Sáenz M., P. Orozco F. y G. Muro P. 2017. Hidrocoria en semillas de Agave victoriae-reginae T. Moore, especie en peligro de extinción: Morfología y anatomía como facilitadores de la hidro-dispersión y germinación. Gayana Botánica 74(2):251-261. Doi:10.4067/S0717-66432017000200251.
Secretaria de Medio Ambiente y Recursos Naturales (Semarnat). 2010. Norma Oficial Mexicana NOM-059-ECOL-2010. Protección ambiental Especies nativas de México de flora y fauna silvestres. Categorías de riesgo y especificaciones para su inclusión, exclusión o cambio. Lista de especies en riesgo. Diario Oficial de la Federación. 30 de diciembre de 2010. México, D.F., México. 40 p.
http://dof.gob.mx/nota_detalle.php?codigo=5173091&fecha=30/12/2010 (5 de agosto de 2020).
Sieber, T. N. 2007. Endophytic fungi in forest trees: Are they mutualist? Fungal Biology Review 21: 75-89. Doi: 10.1016/j.fbr.2007.05.004.
Tropicos. 2019. Tropicos.org. Missouri Botanical Garden. http://www.tropicos.org. (6 de agosto de 2020).
Descargas
Publicado
Versiones
- 31-03-2022 (2)
- 10-01-2022 (1)
Cómo citar
Número
Sección
Licencia
Derechos de autor 2022 Revista Mexicana de Ciencias Forestales

Esta obra está bajo una licencia internacional Creative Commons Atribución-NoComercial 4.0.
Los autores que publiquen en la Revista Mexicana de Ciencias Forestales aceptan las siguientes condiciones:
De acuerdo con la legislación de derechos de autor, la Revista Mexicana de Ciencias Forestales reconoce y respeta el derecho moral de los autores, así como la titularidad del derecho patrimonial, el cual será cedido a la revista para su difusión en acceso abierto.
Todos los textos publicados por la Revista Mexicana de Ciencias Forestales –sin excepción– se distribuyen amparados bajo la licenciaCreative Commons 4.0 Atribución-No Comercial (CC BY-NC 4.0 Internacional), que permite a terceros utilizar lo publicado siempre que mencionen la autoría del trabajo y a la primera publicación en esta revista. (no permite el uso comercial)
Los autores pueden realizar otros acuerdos contractuales independientes y adicionales para la distribución no exclusiva de la versión del artículo publicado en la Revista Mexicana de Ciencias Forestales (por ejemplo, incluirlo en un repositorio institucional o darlo a conocer en otros medios en papel o electrónicos) siempre que indique clara y explícitamente que el trabajo se publicó por primera vez en la Revista Mexicana de Ciencias Forestales.
Para todo lo anterior, los autores deben remitir el formato de carta-cesión de la propiedad de los derechos de la primera publicación debidamente requisitado y firmado por los autores/as. Este formato debe ser remitido en archivo PDF al correo: editorial.forestal@inifap.gob.mx
Esta obra está bajo una licencia de Creative Commons Reconocimiento-No Comercial 4.0 Internacional.





